مهار آدم خواری سلولی برای درمان سرطان

دانشمندان یک معمای قتل سلولی را تقریبا 25 سال پس از سرد شدن پرونده حل کردند. به دنبال شواهدی از مگس میوه گرفته تا موش به انسان نشان داد که سلولهای آدمخوار احتمالاً باعث نقص ایمنی نادر انسان میشوند. اکنون این کشف نویدبخش بهبود درمان سرطان در آینده است.
«این مقاله ما را از زیستشناسی سلولی بسیار بنیادی در یک مگس، به توضیح یک بیماری انسانی و استفاده از آن دانش برای درمان سرطان دنیس مونتل از دانشگاه کالیفرنیا سانتا باربارا گفت: میبرد.» “هر یک از این مراحل به نظر یک کشف بزرگ است، اما اینجا همه آنها در یک مقاله هستند.”
محققان آزمایشگاه Montell یافته های خود را در مجموعه مقالات آکادمی ملی علوم منتشر کردند و اکنون در حال بررسی مکانیسم ها و پیامدهای آن هستند.
یک ژن باستانی
شخصیت اصلی این داستان یک ژن Rac2 و پروتئینی است که آن را رمزگذاری می کند. Rac2 یکی از سه ژن Rac در انسان است. مونتل، نویسنده ارشد، پروفسور داگان و پروفسور برجسته زیست شناسی مولکولی، سلولی و تکاملی میگوید: «راک در تکامل بسیار باستانی است، بنابراین باید عملکردی اساسی داشته باشد».
پروتئین های Rac به ساخت داربست سلولی به نام اسکلت سلولی کمک می کنند. اسکلت سلولی از رشته های پویا ساخته شده است که به سلول ها اجازه می دهد شکل خود را حفظ کنند یا در صورت نیاز تغییر شکل دهند. در سال 1996، هنگام مطالعه گروه کوچکی از سلولها در تخمدان مگس میوه، مونتل به این نتیجه رسید که پروتئینهای Rac در حرکت سلولی مؤثر هستند. از آن زمان، مشخص شد که Rac یک تنظیم کننده تقریبا جهانی برای تحرک سلولی در سلول های حیوانی است .
در دهه 90، او متوجه شد که شکل بیش فعالی از پروتئین Rac1، که تنها در چند سلول در اتاقک تخم مگس بیان می شود، کل بافت را از بین می برد. Abhinava Mishra، نویسنده اصلی این پروژه، دانشمند پروژه در آزمایشگاه Montell توضیح داد: «فقط بیان این Rac فعال در شش تا هشت سلول، کل بافت را که از حدود 900 سلول تشکیل شده است، می کشد.
چرا این اتفاق افتاد؟ چگونه کار می کند؟ مونتل گفت: «این مورد 25 ساله ما بود.
چند سال پیش، شواهدی مبنی بر دخیل خوردن سلولی، همچنین به عنوان آدمخواری، در تخریب بافت شروع شد. یک مرحله در رشد طبیعی تخم مگس وجود دارد که در آن سلولهای خاصی مشابه سلولهای مرزی، همسایههای خود را مصرف میکنند، زیرا دیگر مورد نیاز نیستند. در واقع، آدم خواری سلولی آنطور که انتظار دارید نادر نیست: میلیون ها گلبول قرمز قدیمی در هر ثانیه از بدن انسان حذف می شوند.
Rac2 یکی از اجزای فرآیند پیچیده غذا خوردن است. Rac به سلول در حال خوردن کمک می کند تا هدف خود را بپوشاند. این تیم کنجکاو بود که آیا شکل بیش فعالی از پروتئین باعث می شود سلول های مرزی به طور زودرس همسایگان خود را مصرف کنند.
برای اینکه این اتفاق بیفتد، سلول های مرزی باید اهداف خود را شناسایی کنند که به گیرنده خاصی نیاز دارد. در واقع، زمانی که Mishra این گیرنده را مسدود کرد، سلول های مرزی که Rac فعال شده را بیان می کردند، همسایگان خود را مصرف نکردند و اتاق تخم مرغ زنده و سالم باقی ماند.
مونتل گفت: “مورد سرماخوردگی 25 ساله ما حل شد و این برای ما بسیار راضی کننده بود.” اما این منطقه نسبتاً مهمی از رشد تخم مگس سرکه است. با این حال، پیامدها به زودی رشد خواهند کرد.
یک وضعیت ایمنی مرموز
حول و حوش زمانی که آزمایشگاه او به موفقیت دست یافت، مونتل متوجه یک مطالعه جذاب در مجله خون شد . این مقاله نشان داد که سه فرد غیرمرتبط که از عفونتهای مکرر رنج میبرند، دقیقاً جهش مشابهی داشتند، که Rac2، پروتئین Rac تولید شده در سلولهای خونی را بیش فعال میکند. او مشکوک بود که کشف اخیر آزمایشگاهش در مورد مگس میوه ممکن است این معما را روشن کند.
جهش بیماران فقط در حال فعال شدن خفیف بود، اما کافی بود که همه آنها از چندین عفونت رنج می بردند و در نهایت به پیوند مغز استخوان نیاز داشتند . آزمایشهای خون نشان داد که این بیماران تقریباً هیچ سلول T ندارند، یک نوع تخصصی از گلبولهای سفید خون که برای سیستم ایمنی حیاتی است. این تیم در مؤسسه ملی بهداشت، جهش Rac2 را در موشها وارد کردند و همان از دست دادن مرموز سلولهای T را پیدا کردند. آنها همچنین دریافتند که سلول های T با Rac بیش فعال به طور طبیعی در مغز استخوان حیوانات رشد کرده و به تیموس مهاجرت کرده و در آنجا بدون حادثه به بلوغ خود ادامه می دهند. اما بعداً به نظر می رسید که ناپدید می شوند. بنابراین، مقاله با یک رمز و راز به پایان رسید: چه چیزی باعث ناپدید شدن سلول های T شده است؟
نویسندگان آن مطالعه مجله متوجه شده بودند که بسیاری از نوتروفیل های بیماران – نوع دیگری از گلبول های سفید خون – بزرگ شده بودند. به نظر میرسید که آنها در یک فرد سالم رفتار بسیار زیادی از مواد و رفتار غیرعادی مصرف میکنند.
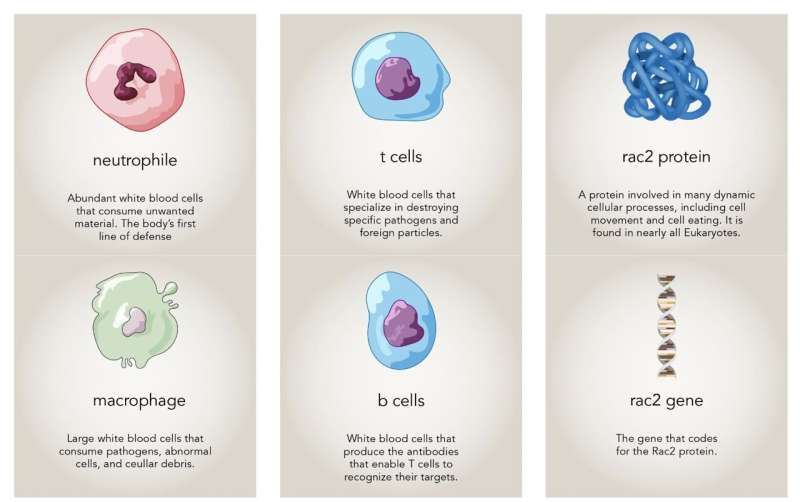
مونتل تعجب کرد که آیا سلول های T بیماران ناپدید می شوند زیرا سلول های ایمنی ذاتی آنها مانند نوتروفیل هایی با Rac2 فعال آنها را می خوردند، دقیقاً مانند سلول های مرزی مگس میوه با Rac فعال که اتاق تخم را می خوردند. تیم او توجه خود را به ماکروفاژها – همتای حریص تر نوتروفیل – برای بررسی معطوف کرد. Mishra ماکروفاژهای انسانی را با و بدون Rac2 بیش فعال همراه با سلول های T کشت داد. او مشاهده کرد که ماکروفاژهای دارای Rac بیش فعال سلول های بیشتری مصرف می کنند و این فرضیه گروه را از کار آنها با مگس میوه تایید می کند.
برای آزمایش اینکه آیا این ممکن است باعث نقص ایمنی مشاهده شده شود، ملانی رودریگز (دانشجوی فارغ التحصیل در آزمایشگاه Montell) از موشهایی با همان جهش بیش فعال Rac2 که در بیماران یافت شد، نمونههای مغز استخوان گرفت. او سپس سلولهای بنیادی مغز را به ماکروفاژها تبدیل کرد و آزمایش مشابهی را با Mishra انجام داد، اما این بار هم ماکروفاژها و هم سلولهای T را با و بدون جهش Rac2 مخلوط کرد .
او دریافت که ماکروفاژها با Rac2 فعال به طور قابل توجهی سلول های T بیشتری نسبت به همتایان عادی خود مصرف می کنند. با این حال، سلول های T با Rac2 فعال نیز نسبت به مصرف هر دو نوع ماکروفاژ آسیب پذیرتر بودند. بنابراین محتمل ترین توضیح برای سلول های T از دست رفته بیماران، ترکیبی از افزایش مصرف توسط ماکروفاژها و همچنین افزایش آسیب پذیری خود سلول های T بود. یک معمای پزشکی انسانی بر اساس مشاهدات اساسی در مگس میوه حل شد.
مهار سلول های وایر
پیامدهای این بینش در ژانویه 2020 گسترش یافت، زمانی که مگان موریسی یکی از نویسندگان این مقاله برای یک مقام هیئت علمی در UCSB مصاحبه کرد. او در سخنرانی خود برنامه ریزی ماکروفاژها برای خوردن سلول های سرطانی را به عنوان یک درمان جدید برای این بیماری توصیف کرد، رویکردی به نام CAR-M. موریسی دریافته بود که افزودن گیرنده CAR به ماکروفاژها این رفتار را ترویج می کند. اما همچنین واضح بود که وادار کردن ماکروفاژها به خوردن بیشتر این رویکرد را مؤثرتر میکند، بهویژه اگر آنها به طور خاص کل سلولهای سرطانی را مصرف کرده و از بین ببرند.
خوب، اگر مونتل و آزمایشگاهش یک چیز را یاد گرفته بودند، این بود که چگونه ماکروفاژها را وادار به خوردن و کشتن سلول های کامل و زنده کنند. بنابراین آنها با موریسی، که اکنون استادیار زیست شناسی مولکولی، سلولی و تکوینی است، همکاری کردند تا تعیین کنند که آیا افزودن Rac2 فعال شده، اثربخشی رویکرد CAR-M را افزایش می دهد یا خیر.
رودریگز ماکروفاژها را از مغز استخوان موشهای نرمال و جهش یافته با Rac2 فعال کرد. در هر یک از این گروهها، موریسی یک گیرنده ساختگی یا گیرنده CAR را بیان کرد که سلولهای B (نوع دیگری از گلبولهای سفید) را تشخیص میدهد. آنها دریافتند که سلول های Rac طبیعی و بیش فعال با گیرنده های ساختگی تعداد زیادی از اهداف سلول B را نمی خورند. همانطور که موریسی قبلا نشان داده بود، ماکروفاژهای طبیعی با گیرنده های CAR سلول های B بسیار بیشتری مصرف می کردند. با این حال، ماکروفاژها با هر دو گیرنده Rac و CAR بیش فعال، دو برابر تعداد سلول های B به اندازه گروه فقط CAR خوردند. Rac2 فعال شده همچنین به نظر میرسید که تعداد به اصطلاح “ابر خواران” را افزایش دهد – ماکروفاژهای درنده که چندین سلول سرطانی را میخورند و میکشند.
نتایج نشان داد که Rac فعال شده و گیرنده هر دو برای اثر افزایش یافته ضروری هستند. Montell توضیح داد: “اگر Rac فعال را بدون گیرنده مناسب اضافه کنید، هیچ کاری انجام نمی دهد.”
این سطح از کنترل، خبر خوبی برای درمانهای بالقوه است، زیرا راهی را به پزشکان میدهد تا حمله ماکروفاژهای اصلاحشده را روی سلولهای سرطانی متمرکز کنند. امیدواریم پزشکان نگران نباشند که سلولهای مهندسیشده سلولهای T بیمار را بخورند، زیرا سلولهای T جهش فعال Rac2 را ندارند که آنها را در برابر این آسیبپذیرتر میکند، همانطور که رودریگز قبلاً کشف کرده بود.
کنونی به نام CAR-T وجود دارد یک درمان سرطان که از گیرنده CAR و سلول های T خود بیمار برای حمله و نابودی سرطان ها استفاده می کند. در برابر برخی سرطان ها بسیار موثر است، اما بسیاری از آنها پاسخ نمی دهند. CAR-M، پسر عموی جدیدتر CAR-T، اخیراً وارد آزمایشات بالینی روی انسان شده است و تا کنون بی خطر به نظر می رسد. مونتل و گروهش علاقه مند به مهار ماکروفاژهای CAR تقویت شده با Rac برای افزایش اثربخشی درمان های CAR-M هستند. آنها حق ثبت اختراع موقت را برای این تکنیک ارائه داده اند-که آنها را اتومبیل اتومبیل می نامند -و از شرکت های بیوتکنولوژی دعوت می کنند تا در توسعه بیشتر این رویکرد شریک شوند.
این مقاله چند وجهی جدید هم سوالات علوم پایه و هم سوالات عملی را مطرح می کند که آزمایشگاه شروع به رسیدگی به آنها کرده است. آنها در حال بررسی این موضوع هستند که آیا این تکنیک ، که در آزمایشگاه بسیار مؤثر است ، در سلولهای ایمنی بدن تازه جمع آوری شده انسان و در مدل های سرطان حیوانات نیز در موش ها و گورخرافی کار خواهد کرد. انجام میدهد این تیم همچنین در حال بررسی این موضوع هستند که Rac2 چگونه این همه را در سطح مولکولی، در اعماق سلولها .
علاوه بر این ، مونتل می خواهد بداند که درمان RaceCar-M با موفقیت ممکن است چند نوع سرطان را هدف قرار دهد. برای مقایسه، CAR-T در برابر سرطان هایی مانند لوسمی و لنفوم موثر بوده است، اما در برابر سرطان های تومور جامد مانند سینه، ریه یا روده بزرگ موثر نیست.
این نتایج مونتل ، یک زیست شناس محترم سلولی را با بیش از 100 مقاله به نام وی متحیر کرده است. وی گفت: “این مقاله مورد علاقه من تاکنون است.”
مونتل افزود : “ما این مورد سرد 25 ساله را در مگس های میوه داشتیم و آن را حل کردیم.” “و این به ما کمک کرد تا رمز و راز یک نقص ایمنی غیر قابل توضیح انسان را حل کنیم. و سپس ما از این دانش برای تقویت ایمونوتراپی بالقوه سرطان استفاده کردیم.
“این فقط یک رمز و راز بعد از دیگری بود ، و RAC معلوم شد که پاسخ هر یک از آنها است.”
اطلاعات بیشتر:
Abhinava K. Mishra و همکاران، Hyperactive Rac، آدمخواری سلول های هدف زنده را تحریک می کند و کشتن سلول های سرطانی با واسطه CAR-M را افزایش می دهد، مجموعه مقالات آکادمی ملی علوم (2023). DOI: 10.1073/pnas.231022112
تهیه شده توسط
دانشگاه کالیفرنیا – سانتا باربارا



